人源化肝臟小鼠模型是如何發(fā)現(xiàn)慢性肝臟疾病?
肝臟,是人體最大的代謝器官,也是維持機體穩(wěn)態(tài)的關(guān)鍵樞紐之一。慢性肝臟疾病,例如酒精性肝病(ALD)和非酒精性脂肪性肝病(NAFLD)、病毒性肝炎、肝臟纖維化和癌癥等,影響著全世界超過15億人...
肝臟,是人體最大的代謝器官,也是維持機體穩(wěn)態(tài)的關(guān)鍵樞紐之一。慢性肝臟疾病,例如酒精性肝病(ALD)和非酒精性脂肪性肝病(NAFLD)、病毒性肝炎、肝臟纖維化和癌癥等,影響著全世界超過15億人。然而,肝臟疾病一直難以在動物模型中進行研究。例如最常用的小鼠模型,其肝臟與人類肝臟有著不同功能。
2023年8月9日,耶魯大學(xué)醫(yī)學(xué)院的研究人員在 Cell 期刊發(fā)表了題為:Humanized mouse liver reveals endothelial control of essential hepatic metabolic functions 的研究論文。
該研究在活體小鼠中創(chuàng)造了一個功能性的人源化肝臟,并發(fā)現(xiàn)了調(diào)控膽固醇水平的人類肝臟特異性機制。這一人源化肝臟小鼠模型可用于評估治療包括非酒精性脂肪性肝病(NAFLD)在內(nèi)的多種慢性肝臟疾病的實驗性藥物的安全性,也有助于找到預(yù)測、預(yù)防和治療各種肝臟疾病的方法。
論文通訊作者、耶魯大學(xué)醫(yī)學(xué)院免疫生物學(xué)教授 Richard Flavell 表示,在肝臟中多種類型的細胞用自己的語言“交流”,而小鼠和人類肝臟細胞用不同的語言“交流”,但這項研究能夠讓人類肝細胞在活體小鼠體內(nèi)用自己的語言“交流”。
肝細胞是人體的主要代謝中樞,執(zhí)行人類特有的功能,在人類疾病中發(fā)生改變,目前認為其功能是通過內(nèi)分泌和細胞自主機制進行調(diào)控的。
在這項研究中,研究團隊使用來自人類肝臟的祖細胞/干細胞和成熟細胞(干細胞)在小鼠模型中“長出”了一個完整人類肝臟,從而創(chuàng)建了一個攜帶人類肝臟組織的小鼠模型。這一人源化肝臟復(fù)刻了人類肝臟結(jié)構(gòu),并且具有與健康人類肝臟類似的細胞功能,執(zhí)行重要的人類特異性代謝/穩(wěn)態(tài)過程,還能模擬人類肝臟病理,包括人類肝臟纖維化和非酒精性脂肪性肝病(NAFLD)。
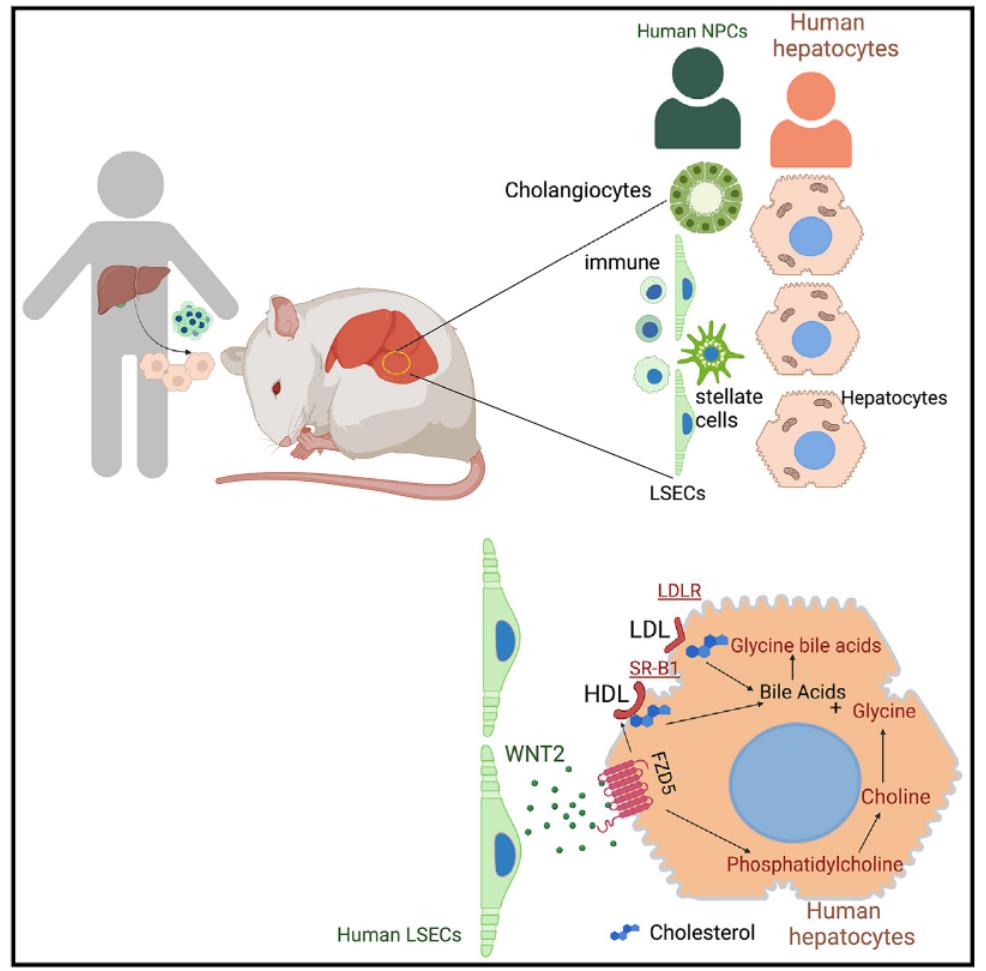
該研究還發(fā)現(xiàn),人類肝細胞的關(guān)鍵代謝功能并非是由肝細胞自主調(diào)控的,而是由微環(huán)境中的非實質(zhì)細胞(NPC)內(nèi)皮細胞所調(diào)控的,內(nèi)皮細胞排列在為肝臟供血的血管上,其以旁分泌的方式調(diào)控人類肝細胞的代謝功能。具體來說,肝竇內(nèi)皮細胞分泌一種名為WNT2的信號分子,通過特異性受體FZD5調(diào)控膽固醇轉(zhuǎn)運到肝細胞以合成膽汁酸,膽固醇轉(zhuǎn)運到肝細胞是降低人體血液中過量膽固醇水平的重要機制。這些結(jié)果揭示了肝臟代謝的基本微環(huán)境調(diào)控及其人類肝臟代謝的特異性。
研究團隊表示,制藥公司可以使用這一人源化肝臟小鼠模型來評估用于治療慢性肝臟疾病的實驗性藥物的安全性。研究團隊的長期目標(biāo)是找到預(yù)測、預(yù)防和治療各種肝臟疾病的方法。
歡迎收藏本站,獲取更多優(yōu)質(zhì)內(nèi)容。如需轉(zhuǎn)載請保留本文地址。本文地址:http://www.zsliqing.cn/article/426.html
- 發(fā)表于 2023-08-12 21:27
- 閱讀 ( 418 )
- 分類:討論熱點
你可能感興趣的文章
- 為什么東莞市被大多數(shù)人認為是掃黃叫雞的地方?一直不理解它的歷史... 250 瀏覽
- 海拔對跑步速度有什么影響? 696 瀏覽
- 個人養(yǎng)老金的實質(zhì)是什么? 228 瀏覽
- “乳糖不耐癥”到底是什么基因引起的? 230 瀏覽
- 為什么海水不適合救火? 509 瀏覽
- 黨委書記和省委書記是平級嗎? 17 瀏覽
0 條評論
請先 登錄 后評論

