【已解決】 為什么兩杯50度的水混在一起不會成為100度?
最佳答案 2025-02-27 00:00
將兩杯50度的水混合后,溫度仍然是50度,而不是100度,這是因為溫度是物體內部分子熱運動的平均動能的量度,而不是熱量的簡單相加。以下是詳細的解釋:
1.?溫度的本質
溫度反映了物質內部分子的平均動能。當兩杯50度的水混合時,它們的分子動能會通過碰撞達到平衡,但平均動能并不會翻倍,因此溫度不會升高到100度。
2.?熱力學第一定律
混合過程中,系統的總熱量保持不變(假設沒有能量損失)。兩杯水的熱量相加后,總熱量分配到更大的質量中,導致溫度不變。公式表示為:
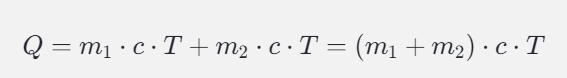
因此,混合后的溫度仍為T(50度)。
3.?實際類比
- 疊加誤解:溫度不是可疊加的物理量。例如,兩塊20度的金屬塊接觸后,溫度仍是20度,不會變成40度。
- 能量分布:熱量會從高溫傳向低溫,直到平衡。混合兩杯同溫度的水時,系統已處于平衡狀態,溫度不變。
4.?極端情況
即使混合更多50度的水,溫度仍保持50度,因為熱量均勻分布到更大的質量中。
總結
溫度是分子動能的平均體現,混合相同溫度的水只會保持原溫度,而不會疊加。100度的水需要通過外部加熱(如燃燒)額外提供能量,而不是簡單混合。
請先 登錄 后評論
感謝您的支持,請隨意打賞。您的贊賞將鼓勵我繼續創作!

百科搬運工
- 行走的百科全書
- 1 關注
- 0 收藏,450 瀏覽
- 匿名 提出于 2025-02-24 09:12
掃碼關注微信公眾號

相似問題
- 金星為什么沒有磁場? 1 回答
- 網上哪個平臺能買到絡新婦蜘蛛? 1 回答
- 暴龍恐龍的生活習性如何? 1 回答
- 古羽龍恐龍的外形特征? 1 回答
- 大盜龍恐龍的滅絕原因? 1 回答
- 湖泊龍分布哪些地區? 1 回答